|
La valvulopatia aortica nell’Anziano e nel Grande Anziano: epidemiologia e clinica
Rodolfo Citro, Costantina Prota, Angelo Silverio, Giovanni Vitale, Marco Di Maio, Armando Cavallo. Dipartimento “Cuore” – A.O.U. San Giovanni di Dio e Ruggi d’Aragona, Salerno
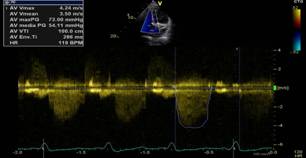
Le dimensioni del problema Con il progressivo invecchiamento della popolazioneche si è registrato negli ultimi decenni nelle società occidentali, le valvulopatie cardiache sono diventate un importanteproblema di salute pubblica,contribuendo all’incremento di morbilità e mortalità per cause cardiovascolari nei pazienti anziani1.Diversi studi epidemiologici hanno riscontrato che più di una persona su otto oltre i 75 anni d’età soffre di una malattia valvolare cardiaca di grado moderato o severo,e tale dato potrebbe addirittura essere ancora sottostimato2. In particolare, la stenosi aortica (SA) è diventata lavalvulopatia più frequente in Europa e nel Nord America1,3. La causa più comune è rappresentata dalla forma degenerativa calcifica (denominata anche stenosi aortica senile o sclerocalcifica); la seconda causa più frequente, soprattutto nei soggetti più giovani, è rappresentata dalla stenosi aortica congenita; infine vi è l’eziologia reumatica, ormai divenuta rara nei paesi occidentali ma ancora ben rappresentata nei paesi in via di sviluppo4. La metodica di scelta per la diagnosi ed il successivo follow up della SA è rappresentata dall’ecocardiografia, che fornisce informazioni dettagliate circa l’anatomia della valvola, l’eziologia e la severità della stenosi ed infine l’impatto della valvulopatia sulla funzionalità del ventricolo sinistro. Combinando i dati dell’area valvolare aortica e del gradiente di pressione transvalvolareè possibile classificare la SA in lieve, moderata o severa. La SA è considerata severa quando presenta un’area valvolare aortica < 1cm2 e un gradiente di pressione transvalvolare medio > 40 mmHg5.Bisogna considerare però anche forme particolari di SA: - la SA severa a basso flusso/basso gradiente (in cui la ridotta area valvolare è associata ad un gradiente medio transvalvolare< 40 mmHg a causa della ridotta frazione di eiezione); - la SA pseudo-severa ( in cui l’area orifiziale è ridotta solo funzionalmente e non morfologicamente a causa della bassa portata cardiaca);
Poiché non
esiste un trattamento farmacologico in grado di rallentare o
invertire il decorso della SA, l’intervento cardiochirurgico di
sostituzione valvolare aortica con protesi meccaniche o
biologiche costituisce lo standard terapeutico della SA severa6.
Molti Una recente metanalisi ha valutato non solo la prevalenza della stenosi aortica nell’anziano ma anche il numero di pazienti attualmente candidabili a procedura TAVI, analizzando sette studi inerenti l’epidemiologia di tale condizione nella popolazione anziana dell’Europa e del Nord America; è risultato quindi che la prevalenza di SA nei soggetti con età ≥75 anni è del 12.4 %, di cui il 3.4 % è affetto da SA di grado severo. E stato inoltre calcolato che circa 290000 pazienti con SA severa ad alto rischio chirurgico possono essere potenzialmente trattati con la TAVI, e che ogni anno vi sono circa 27000 nuovi pazienticandidabili a tale procedura8.
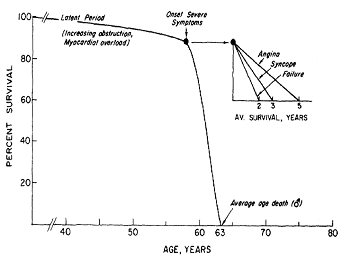
Quando intervenire? La stenosi valvolare aortica è una condizione patologica a decorso progressivo e potenzialmente letale. Essa infatti comporta, a causa dell’ aumentata resistenza all’eiezione del sangue, un sovraccarico pressorio del ventricolo sinistro che sviluppa inizialmente un’ipertrofia concentrica compensatoria, mantenendo per anni una normale funzione di pompa, fino all’insufficienza funzionale9. Dopo l’insorgenza dei sintomi (dispnea, angina, sincope), la prognosi per i pazienti non trattati è estremamente severa: peggioramento continuofino alla morte. Nello specifico, la durata media di vita in assenza di sostituzione valvolare è di 3-5 anni dopo insorgenza di angina pectoris, 2-3 anni dopo la prima sincope e 2 anni dopo il primo episodio di scompenso cardiaco10 . Inoltre la percentuale media di sopravvivenza, dopo l’insorgenza dei sintomi, è del 50% a due anni e del 20% a cinque anni11. In base a questi dati l’European Society of Cardiology e l’ EuropeanAssociation for Cardio-ThoracicSurgery (ESC/EACTS) hanno raccomandato l’intervento di sostituzione valvolare nei pazienti con SA severa sintomatici per angina, sincope o scompenso cardiaco (Classe di Raccomandazione I, livello di evidenza B). Ulteriore indicazione è stata posta nei pazienti con SA severa che devono essere sottoposti a by-pass coronarico o ad altri interventi cardiochirurgici sull’aorta ascendente o su altre valvole cardiache (Classe IC). Il trattamento dei pazienti con SA severa ma asintomatici nelle loro attività quotidiane resta tuttora controverso: recenti studi infatti non raccomandano l’intervento chirurgico in tutti i pazienti in questa condizioneperchè i rischi globali dell’intervento di sostituzione valvolare sono significativamente superiori al beneficio atteso in termini di prevenzione della morte improvvisa. La decisione deve scaturire caso per caso da un’attenta analisi del rapporto rischio/beneficio. Comunque le linee guida ESC/EACTS pongono in classe IC l’indicazione all’intervento di sostituzione valvolare per i pazienti con SA severa asintomatica con severa disfunzione del ventricolo sinistro (FE<50%) e i pazienti asintomatici con ECGda sforzo positivo6.
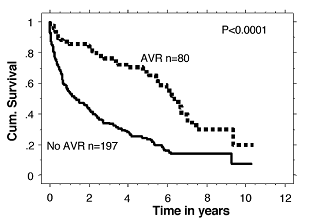
La sostituzione chirurgica della valvola aortica ha prodotto risultati eccellenti negli ultimi anni, con una mortalità molto bassa, prolungando la vita dei pazienti e migliorandone la qualità6. L’età non è da considerare di per sè una controindicazione alla chirurgia, anzi persino nei pazienti ultraottantenni gli esiti funzionali si sono rivelati eccellenti a seguito dell’intervento di sostituzione valvolare12. Paragonata alla terapia medica, la sostituzione valvolare chirurgica presenta percentuali di sopravvivenza maggiori anche nei pazienti ultraottantenni (87, 78 e 68% rispettivamente a 1,2 e 5 anni nei pazienti sottoposti a chirurgia vs 52, 40 e 22% rispettivamente a 1,2 e 5 anni nei pazienti non sottoposti ad intervento)13. Tuttavia, i pazienti anziani sono spesso affetti da una serie di altre comorbidità(diabete, insufficienza renale cronica, broncopneumopatia cronica ed altre malattie concomitanti) che incrementano il rischio di complicanze durante e dopo l’intervento chirurgico14. I principali fattori di rischio associati ad incremento della mortalità a breve e lungo termine in seguito all’intervento chirurgico sono risultati: età avanzata, sesso femminile, Classe NYHA alta, disfunzione sistolica ventricolare, ipertensione polmonare, coronaropatia, pregresso intervento cardiochirurgico, aritmie ventricolari6.Al fine di quantificare il rischio cardiochirurgico individuale, diversi predittori indipendenti di mortalità precoce dopo intervento di sostituzione valvolare aorticasono stati inseriti in vari sistemi di calcolo per ottenere un punteggio circa il rischio effettivo, il piu importante dei quali è l’EuroSCORE(European System for Cardiac Operative Risk Evaluation)15.Controindicazioni principali all’intervento sono le condizioni cliniche generali scadenti, un’aspettativa di vita inferiore a un anno, insufficienza renale o epatica, eventi cerebrovascolari,ridotta riserva cardiocircolatoria per coronaropatia o broncopneumopatiacronica ostruttiva, sepsi, endocardite, fibrillazione atriale, tromboembolie, diatesi emorragica, aneurismaaortico, condizioni che rendono impossibile la circolazione extracorporea o l’approccio chirurgico sternaleper interventi pregressi6.
La TAVI,
introdotta nel 2002, è diventata dunque un’allettante
alternativa terapeutica soprattutto nei pazienti anziani grazie
alla sua minore invasività rispetto all’intervento
cardiochirurgico.Oggi sono gia’ disponibili due diverse protesi
impiantabili per via transcatetere: la Corevalve della
Medtronic, autoespandibile, e la Sapien della Edwards,
balloon-expandable. Il primo e più importante studio condotto
nel mondo delle valvole cardiache transcatetere è stato il
PARTNER trial (TranscatheterAortic-Valve Implantation for
AorticStenosis in PatientsWhoCannotUndergoSurgery). Il PARTNER
trial coinvolge due gruppidi pazienti studiate separatamente: la
coorte A comprende 699 persone in cui la TAVI viene paragonata
alla sostituzione chirurgica della valvola aortica; la coorte B
comprende 358 pazienti in cui la TAVI viene invece paragonata
alla terapia medica standard, compresa la valvuloplastica nel 40
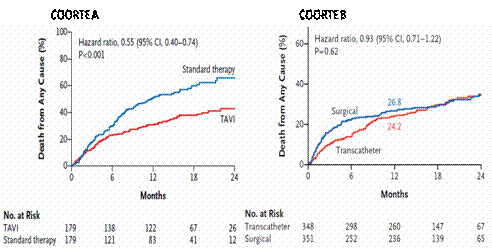
% dei pazienti.Paragonata alla terapia medica, la TAVI ha
mostrato un grande vantaggio in termini sia di mortalita’
(30.7% vs 50.7% ) che di mortalita’ e riospedalizzazioni
(71.6% vs 42.5%). La TAVI e l’intervento chirurgico di
sostituzione valvolare aortica hanno mostrato gli stessi tassi
di mortalità da tutte le cause ad un anno (24.2 % vs 26.8%
rispettivamente), affermando la non inferiorità della procedura
percutanea rispetto all’intervento standard. La procedura
percutanea non è però esente da possibili complicanze: le più
frequenti sono risultate lo stroke, il blocco atrio-ventricolare
richiedente l’impianto di pacemaker, le perforazioni cardiache
e/o vascolari e i leakperiprotesici.Complicanze
neurologiche ( stroke e attacco ischemico transitorio)si sono
verificate più frequentemente nel gruppo TAVI rispetto al gruppo
chirurgia tradizionale sia a 30 giorni (5.5% vs 2.4%) che ad 1
anno (8.3% vs 4.3%); così comecomplicanze vascolari maggiori
sono risultate più frequenti nel gruppo TAVI (11.3% vs 3.5% ad 1
anno). Per quanto riguarda invece episodi di sanguinamento
maggiore (14.7% vs 25.7% ad 1 anno) e insorgenza di
fibrillazione atriale (12.1% vs 17.1% ad 1 anno), queste sono
stati più frequenti nel gruppo chirurgia tradizionale rispetto
al gruppo TAVI.
La metanalisi di Tsukui et al.18 ha analizzato una serie di precedenti studi sulla stenosi aortica severa nei pazienti con età ≥ 80 anni e riportato anche una casistica personale di 1051 pazienti sottoposti ad intervento cardiochirurgico di sostituzione valvolare. L’ intervento chirurgico è asscoiato a una mortalità parial 2.4- 6.8 % a seconda dello studio considerato; inoltre la percentuale di sopravvivenza tra pazienti “anziani” e pazienti con età inferiore sottoposti ad interventocardiochirurgico sono risultati molto simili in tutti gli studi analizzati, nonostante la maggiore incidenza di complicanze post-chirurgiche (in particolare stroke, TIA, insufficienza renale, fibrillazione atriale) nel gruppo di pazienti più anziani. Si conferma dunque che l’intervento chirurgico di sostituzione valvolare rappresenta la scelta ottimale per la SA severa anche nei pazienti anziani. Per quanto riguarda la TAVI, anche da questo studio si evince la non inferiorità di tale metodica rispetto alla chirurgia nei pazienti anziani; tuttavia si rileva la maggiore frequenza di complicanze vascolari ( dissezione, ematoma nel sito di accesso, perforazione, emorragie) e di leakperiprotesici nei pazienti sottoposti a TAVI rispetto ai pazienti sottoposti ad intervento chirurgico standard. Lo studio effettuato da Im et al.19 ha comparato gli outcomes precoci di un un gruppo di pazienti coreani con età ≥80 anni suddivisi in tre sottogruppi: 10 pz sottoposti a TAVI, 14 a chirurgia, 42 a terapia medica ottimale. Il risultato principale di tale studio è stato che gli eventi avversi maggiori cardiovascolari e cerebrovascolari durante il follow-up a tre mesi sono risultati molto meno frequenti nel gruppo di pz sottoposti a TAVI rispetto al gruppo sottoposto a chirurgia e quello sottoposto a terapia medica ottimale ( 0% vs 50% vs 42.9%). E stata quindi confermata l’efficacia e la sicurezza della procedura percutanea, tanto che lo studio conclude che la TAVI dovrebbe essere consideratala tecnica di prima scelta nel trattamento di pazienti ultraottantenni con SA sintomatica severa. Conclusioni Nel trattamento della stenosi aortica severa sintomatica nei pazienti anziani è necessario un approccio multidisciplinare da parte del cosiddetto “heart team” per indirizzare ogni paziente verso la migliore opzione terapeutica20. La TAVI,nonostante gli ottimi risultati, rappresenta ancora una alternativa allaclassica chirurgia di sostituzione valvolare, che resta ancora la terapia di elezione. La FIC e la SICCH hanno elaborato un documento di consenso che prevede l’impianto in soggetti di eta’>75 anni e Euroscore>20% oppure >85 anni e Euroscore>10%21. Tuttavia sono ancora numerosi gli aspetti da chiarire: - la corretta selezione dei pazienti candidabili all’impianto percutaneo: - la prevenzionee gestione delle complicanze peri-procedurali; - l’assenza di dati di follow up prolungati, data l’introduzione recente della metodica. È possibile che in un futuro non lontano sempre più pazienti possano essere sottoposti a TAVI. Occorreranno, tuttavia, studi di confronto a lungo terminetra TAVI e chirurgia nei pazienti anzianiper avere le evidenze necessarie a definire con maggiore precisione le indicazioni di queste due procedure.
Bibliografia
1. Nkomo VT, Gardin JM, Skelton TN et al. Burden of valvular heart diseases: a population-based study. Lancet 2006; 368:1005-11. 2. National Heart Lung and Blood Institute, U.S. National Institutes of Health. Heart Valve Disease. November 12, 2010. 3. Iung B, Baron G, Tornos P et al. Valvular heart disease in the community: A European experience. CurrProblCardiol 2007;32:609-661. 4. Iung B, Baron G, Butchart EG et al. A prospective survey of patients with valvular heart disease in Europe: The Euro Heart Survey on Valvular Heart Disease. EurHeart J. 2003 Jul;24(13):1231-43. 5. Baumgartner H, Hung J, Bermejo J et al. Echocardiographicassessment of valvestenosis: EAE/ASE recommendations for clinical practice. Eur J Echocardiogr. 2009 Jan;10(1):1-25. 6. Vahanian A, Alfieri O, Andreotti F, et al. Guidelines on the management of valvular heart disease. EurHt J 2012. Aug 24. 7. Pierard S, Seldrum S, de Meester C, et al. Incidence, determinants, and prognostic impact of operative refusal or denial in octogenarians with severe aortic stenosis. Ann Thorac Surg. 2011;91:1107–12. 8. Osnabrugge RL, Mylotte D, Head SJ et al. Aortic Stenosis in the Elderly: Disease Prevalence and Number of Candidates for Transcatheter Aortic Valve Replacement: A meta-analysis and modelling study. J AmCollCardiol. 2013 Sep 10;62(11):1002-12. 9. Otto M. Valve disease: timing of aortic valve surgery. Heart2000;84:211–218. 10. Ross J Jr, Braunwald E. Aortic Stenosis. Circulation 1968; 38(suppl 1):61-7. 11. Lester SJ, Heilbron B, Gin K, et al. The natural history and rate of progression of aortic stenosis. Chest1998; 113:1109-14. 12. Sundt TM, Bailey MS, Moon MR, et al. Quality of life after aortic valve replacement at the age of >80 years. Circulation2000; 102[suppl III]:III-70-111-74. 13. Varadarajan P, Kapoor N, Bansal RC et al. Survival in elderly patients with severe aortic stenosis is dramatically improved by aortic valve replacement: Results from a cohort of 277 patients aged > or =80 years.Eur J CardiothoracSurg. 2006 Nov;30(5):722-7. 14. Iung B, Cachier A, Baron G, et al. Decision making in elderly patients with severe aortic stenosis: why are so many denied surgery? Eur Heart J 2005;26:2714-20. 15. Ambler G, Omar RZ, Royston P, et al. Generic, simple risk stratification model for heart valve surgery. Circulation 2005;112:224-31. 16. Smith CR, Leon MB, Mack MJ, et al. Transcatheter versus Surgical Aortic-Valve Replacement in High-Risk Patients.N Engl J Med. 2011 Jun 9;364(23):2187-98. 17. Leon MB, Smith CR, Mack M, et al. Transcatheter aortic-valve implantation for aortic stenosis in patients who cannot undergo surgery. N Engl J Med2010; 363:1597-1607. 18. Tsukui H, Yamazaki K. Contemporary strategy for aortic valve stenosis in octogenarians. SurgToday. 2013 Jul 14. 19. Im E, Hong MK, Ko YG, et al. Comparison of Early Clinical Outcomes Following Transcatheter Aortic Valve Implantation versus Surgical Aortic Valve Replacement versus Optimal Medical Therapy in Patients Older than 80 Years with Symptomatic Severe Aortic Stenosis.YonseiMed J. 2013 May 1;54(3):596-602. 20. Vahanian A, Alfieri O, Al-Attar N et al: Transcatheter valve implantation for patients with aortic stenosis: a position statement from the European Association of Cardio-Thoracic Surgery (EACTS) and the European Society of Cardiology (ESC), in collaboration with the European Association of Percutaneous Cardiovascular Interventions (EAPCI) Eur Heart J 2008 29, 1463–1470 21. Santoro G, Vitali E, Tamburino C et al : Impianto transcatetere di protesi valvolare aortica in pazienti con stenosi valvolare severa sintomatica Documento di Consenso Federazione Italiana di Cardiologia (FIC) - Società Italiana di Chirurgia Cardiaca (SICCH) G ItalCardiol 2010; 11: 45-53
|