|
Il trattamento chirurgico DELLE STENOSI DELLA CAROTIDE E delLE ARTERIOPATIE PERIFERICHE.
Eugenio Meucci, Luigi Meucci, Alessandro Luongo, Adriana Perziano, Salvatore De Vivo U. O. C. di Chirurgia Vascolare PO S.Luca – Vallo della Lucania Dipartimento Cardiovascolare ASL SA 3
La possibilità di un trattamento endoluminale interessa ormai tutte le arteriopatie extracoronariche e il punto di vista del chirurgo vascolare non può essere diverso da quello di altri operatori (interventisti e non) con i quali si confronta e collabora quotidianamente. Gli elementi di maggiore difficoltà sono attualmente rappresentati dalla standardizzazione delle indicazioni al trattamento e dalla scelta sempre più difficile tra le due modalità terapeutiche di cui disponiamo, endovascolare e chirurgica convenzionale, spesso senza poter disporre di criteri precisi. Quali sono gli elementi che ci indirizzano nel trattamento delle stenosi carotidee e dell'arteriopatia ostruttiva cronica degli arti inferiori?
STENOSI CAROTIDEE L'ictus cerebrale rappresenta la terza causa di morte nei paesi industrializzati e la principale causa di invalidità permanente con una prevalenza nella popolazione anziana (età>65 anni) del 6,5% (M>F). I trials pubblicati (NASCET ed ECST per le stenosi sintomatiche, ACAS ed ACST per le stenosi asintomatiche) hanno dimostrato l'efficacia dell’endoarteriectomia carotidea rispetto alla terapia medica nella prevenzione dell'ictus ischemico, definendo con chiarezza le indicazioni della chirurgia nei pazienti sintomatici e asintomatici, con un livello di evidenza I e un grado di raccomandazione A. E' ampiamente dimostrato come il massimo beneficio, in termini di prevenzione di eventi ischemici, si abbia nei pazienti sintomatici nei quali la riduzione di rischio è riscontrabile per stenosi superiori al 70% e, anche se meno evidente, per stenosi superiori al 50%, a condizione di mantenere il tasso di complicanze perioperatorie al di sotto del 6%. Recenti metanalisi hanno confermato come il beneficio sia direttamente proporzionale al grado di stenosi (ad eccezione delle pseudo-occlusioni o near-occlusion), proponendo in aggiunta altri fattori prognostici indipendenti: età, sesso, caratteristiche della placca, natura del sintomo (oculare o emisferico), data dell'evento ischemico. In relazione al fattore temporale è infatti attualmente riconosciuto che nelle stenosi sintomatiche il beneficio dell'intervento è inversamente proporzionale al tempo trascorso dal sintomo. Nei pazienti che hanno sviluppato TIA ed ictus minori si ritiene attualmente indicata difatti l'endoarterectomia precoce, cioè entro le prime due settimane dall'evento clinico (Raccomandazione di grado A). In relazione alla stenosi asintomatica l'intervento è indicato nelle stenosi di grado maggiore del 60% (valutata con il metodo NASCET) a condizione che il tasso di morbi-mortalità sia inferiore al 3%. La riduzione assoluta di rischio di ictus è, in tal caso, modesta (1%/anno), ma statisticamente significativa a cinque anni. E' auspicabile, pertanto, nei pazienti asintomatici, una revisione sistematica che stratifichi i vari fattori di rischio, onde identificare i sottogruppi a maggiore rischio di ictus nei quali è maggiore il beneficio del trattamento chirurgico (grado di stenosi, caratteristiche della placca, sesso maschile, ipercolesterolemia, ipercreatininemia). Facendo riferimento alla prognosi a lungo termine, il rischio annuale di ictus omolaterale di questi pazienti portatori di stenosi asintomatica rimane nell'ordine del 2%, sensibilmente inferiore quindi al rischio di infarto miocardico e di morte vascolare non correlata ad ictus. Si impone pertanto primariamente un intervento globale di prevenzione. Il ruolo dell'endoarterectomia nel trattamento della stenosi carotidea è stato rimesso in discussione in questi ultimi anni dalla diffusione dello stenting carotideo che si propone attualmente come una procedura quanto mai attraente, che consente di ottenere un risultato morfologico soddisfacente nel caso di lesioni anatomicamente favorevoli. Si pone peraltro il difficile problema della selezione dei pazienti sulla base di criteri ancora non ben definiti. Le attuali evidenze non sono, però, tali da suggerire un cambio di tendenza dall'endoarterectomia verso lo stenting nel trattamento routinario della stenosi carotidea (Raccomandazione di grado A). Lo stenting carotideo, con adeguati livelli di qualità procedurale ed adeguata protezione cerebrale è indicato in caso di gravi comorbidità cardiache o polmonari ed in condizioni specifiche come la paralisi del ricorrente controlaterale, stenosi ad estensione craniale o caudale ritenute inaccessibili (Raccomandazione di grado B). Per convenzione le gravi comorbidità cardiache si intendono: lo scompenso cardiaco, un intervento cardiochirurgico nelle sei settimane precedenti, un infarto miocardico nelle quattro settimane precedenti e l'angina instabile. Lo stenting carotideo è indicato, inoltre, in caso di condizioni specifiche (restenosi, stenosi post-attiniche, colli ostili, occlusione controlaterale) (Raccomandazione di grado C). In realtà la definizione di pazienti a rischio per un intervento di endoarterectomia carotidea non è affatto scontata. Numerose casistiche riportano infatti risultati del tutto soddisfacenti con l’endoarterectomia carotidea anche in pazienti con quelle lesioni anatomiche ovvero con quelle comorbidità che li definirebbero ad “alto rischio chirurgico”. Basti pensare che l’età superiore a 80 anni nei risultati preliminari del CREST ed in altre revisioni risulta un fattore di rischio elevato dello stenting carotideo, non già dell’ endoarterectomia carotidea. Cionondimeno, pur mancando una “evidenza” scientifica che giustichi la diffusione che lo stenting sta conoscendo, i suoi risultati, man mano che il volume delle procedure e quindi l’esperienza acquisita aumentano, sono sempre più incoraggianti. Molti sono quindi gli operatori che impiegano routinariamente l'angioplastica carotidea e piuttosto che individuare i pazienti ad alto rischio chirurgico da indirizzare verso il trattamento endovascolare, tendono ad individuare le lesioni anatomiche a rischio per uno stenting da indirizzare verso l’endoarterectomia carotidea. I rischi dell’angioplastica carotidea sono infatti legati essenzialmente a taluni aspetti anatomici sfavorevoli o proibitivi che possono condurre al suo insuccesso quali: · l’ esistenza di placche calcifiche e emboligene a livello dell’ arco aortico ; · talune conformazioni dell’arco e dei tronchi epiaortici ; · l’ esistenza di lesioni ostiali che rendono il cateterismo selettivo “a rischio” ; · il carattere particolarmente serrato della placca carotidea e soprattutto la sua morfologia che condiziona il rischio emboligeno (lesioni ipoecogene, materiale trombotico); · e infine le tortuosità accentuate della carotide interna. Resta, però, ancora da dimostrare se l’angioplastica carotidea, al di là dei pazienti “a rischio” , possa essere proposta anche in pazienti a “basso rischio “ chirurgico, se sia in grado di assicurare a distanza l’indennità anatomica, cioè la pervietà dell’asse carotideo, e l’indennità neurologica del paziente, cioè la prevenzione dell’ictus che è l’unico vero scopo del trattamento delle lesioni carotidee. I dati attualmente disponibili confermano, in conclusione, che l'endoarterectomia è ancora il trattamento di scelta delle stenosi carotidee secondo le indicazioni dei trials ormai “storici” i cui risultati si sono dimostrati ormai largamente riproducibili. L'angioplastica andrebbe riservata a pazienti arruolati in trial clinici ovvero a pazienti ad “alto rischio” con tutte le riserve che la definizione di “alto rischio” comporta. Siamo in attesa dei risultati dei trials ancora in corso perché trovi conferma o meno la convinzione di molti di noi che l’angioplastica carotidea possa avere delle indicazioni ben più larghe di quelle attuali.
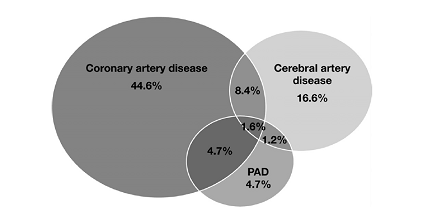
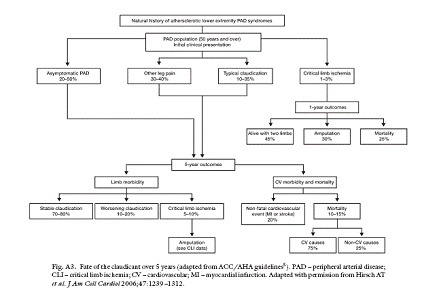
ARTERIOPATIE ARTI INFERIORI A noi tutti è noto come il paziente affetto da un’arteriopatia cronica ostruttiva a carico degli arti inferiori presenti un elevato rischio di altre complicanze cardiovascolari, ben più gravi del suo disturbo funzionale, e quanto siano pertanto cruciali il controllo dei fattori di rischio, il trattamento antiaggregante piastrinico e un programma di riabilitazione, sulla cui necessità occorre assolutamente sensibilizzare in prima istanza il paziente.
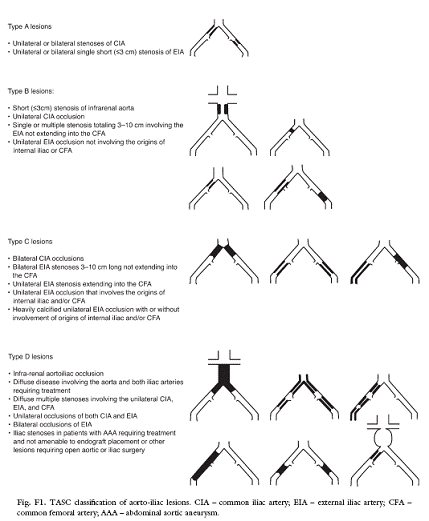
Solo allora si può discutere l’indicazione a una rivascolarizzazione ricorrendo ad una soluzione chirurgica tradizionale, endovascolare o ibrida, scelta questa che se talora è evidente, spesso è difficile non esistendo dati in letteratura che consentano di precisarne le rispettive indicazioni. La scelta deve tener conto di diversi elementi: · l’ entità della sintomatologia del paziente, relativa alle proprie esigenze funzionali; · il profilo anatomico delle lesioni, la loro sede, estensione e natura; · i rischi; · i risultati a distanza delle diverse metodiche di rivascolarizzazione ; · il contesto clinico del paziente e le sue aspettative di vita. Relativamente al profilo anatomico delle lesioni tale scelta viene senz’altro indirizzata dalla classificazione TASC (Trans-Atlantic Inter-Society Consensus) che ha distinto in quattro tipi diversi le lesioni obliteranti aorto-iliache, femoro-poplitee ed infrapoplitee. Per la localizzazione aorto-iliaca, a seconda che si tratti di stenosi o di occlusioni, di lesioni corte o estese, dell’iliaca comune, esterna o di entrambe, sono stati distinti 4 tipi di lesioni A,B,C e D che vedete qui dettagliati e schematicamente rappresentati. Le lesioni di tipo A, meno severe, sono più volentieri suscettibili di un trattamento endoluminale, quelle di tipo D di un trattamento chirurgico, mentre per le lesioni di grado intermedio, di tipo B e C, la scelta dipende dall'età e dal profilo di rischio del paziente, dalle comorbidità, ma viene significativamente influenzata dall’esperienza e dalle preferenze dell’operatore. Resta il dato che in un’analisi del Nationwide Inpatient Sample negli Stati Uniti tra il 1996 e il 2000 si è osservato un incremento di 8 volte del numero delle angioplastiche iliache, da 0.3% a 3.4% ogni 100.000 adulti, mentre il numero dei bypass aorto-femorali è diminuito del 15.5%, da 5.8% a 4.9% ogni 100.000 adulti.
Le rivascolarizzazioni chirurgiche aorto-femorali vengono attualmente realizzate il più delle volte con bypass protesici con risultati in termini di pervietà immediata e a distanza di gran lunga migliori che nel passato, grazie alla messa a punto di tecniche sempre più meticolose e precise. Le rivascolarizzazioni «ideali» a livello aorto-iliaco sono i bypass anatomici, ma in pazienti a rischio una soluzione alternativa, meno aggressiva, viene offerta dai bypass extraanatomici, il cui tragitto è sottocutaneo, e che quindi evitano sia la laparotomia che il clampaggio aortico. Il bypass aorto-femorale è attualmente indicato nel caso di : · lesioni aortiche non suscettibili di un trattamento endoluminale, quali le stenosi calcifiche e le occlusioni juxta-renali ; · lesioni iliache associate a un aneurisma o a una distrofia aneurismatica dell’ aorta. · stenosi o occlusioni multiple dell’iliaca comune, dell’iliaca esterna e eventualmente della biforcazione femorale ; · occlusione di entrambe le iliache esterne. I risultati immediati e a distanza della chirurgia aorto-iliaca sono ben noti. Da una meta-analisi relativa a 23 pubblicazioni ed alcune migliaia di pazienti la pervietà a 5 e a 10 anni è eccellente, essendo, rispettivamente, del 91 e dell’86% per i pazienti con claudicatio, e dell’87 e 82% per i pazienti con ischemia critica. L’aspetto più interessante dei progressi di questa chirurgia è la netta riduzione della mortalità che attualmente è del 2-5% e che trova le sue ragioni in quelle misure di protezione miocardiche che in questi ultimi due decenni sono state oggetto di una ricerca clinica estremamente interessante e che consistono da un lato nello screening e nell’eventuale trattamento delle lesioni coronariche associate, dall’altro nella protezione farmacologica nel periodo peri-operatorio. Quanto ai bypass extra-anatomici, il bypass axillo-femorale e femoro-femorale, proposti inizialmente nei pazienti a alto rischio in alternativa alla chirurgia diretta dell’aorta, hanno attualmente indicazioni limitate, poiché da un lato, come già menzionato, lo sviluppo delle metodiche endoluminali ha globalmente ridotto le indicazioni a una rivascolarizzazione chirurgica delle lesioni obliteranti aorto-iliache, dall’altro la riduzione delle complicanze cardiache ha ridotto il numero dei pazienti a rischio nei quali una chirurgia aortica diretta è controindicata. Il bypass axillo-femorale ha una pervietà a 5 anni che oscilla nelle diverse casistiche tra il 35% e l’85%, ma che in ogni caso è nettamente inferiore a quella dei bypass aorto-femorali. Pertanto, attualmente è impiegato unicamente in un contesto d'urgenza o nel caso di pazienti ad “alto rischio”, con aspettative di vita limitate, in ischemia critica le cui lesioni non siano suscettibili di un trattamento endoluminale. I risultati del bypass femoro-femorale sono nettamente migliori, con una pervietà a 5 anni che varia tra il 55% e il 70% nelle diverse casistiche anche se il rischio evolutivo di lesioni obliteranti sull’asse iliaco “donatore” lascia comunque propendere, qundo possibile, per una chirurgia diretta aorto-femorale. Nel distretto femoro-popliteo, ed infrapopliteo i risultati delle rivascolarizzazioni (chirurgiche o endovascolari) sono, invece, meno soddisfacenti che a livello aorto-iliaco suggerendo, pertanto, una restrizione delle indicazioni chirurgiche quasi esclusivamente a pazienti in ischemia critica. Nei casi in cui si intervenga per una claudicatio invalidante ancora più importante è un'attenta valutazione del contesto clinico e del quadro anatomico commisurando i rischi procedurali con in tassi di pervietà immediati ed a distanza della procedura proposta, evitando ad ogni costo rivascolarizzazione iuxta o sotto-articolari. Si pone quindi ancora una volta la scelta tra una rivascolarizzazione chirurgica convenzionale, o un trattamento endoluminale. La scelta come per le lesioni obliteranti aorto-iliache deve tener conto del tipo di lesione. Anche le lesioni obliteranti femoro-poplitee ed infrapoplitee sono state distinte in quattro diversi tipi, A, B, C, D, in funzione del grado delle lesioni, stenosi o occlusione, che si tratti di lesioni isolate o multiple, dell’estensione delle lesioni, inferiori o superiori a 3 cm o a 5 cm, della localizzazione o meno a livello della femorale comune, dell’origine della femorale superficiale o a livello della biforczione poplitea, del carattere calcifico o meno delle lesioni. Ancora una volta, le lesioni meno severe, il tipo A, le stenosi corte e segmentarie, sarebbero favorevoli a un trattamento endoluminale, quelle più estese, le D, le occlusioni femoro-poplitee, al trattamento chirurgico convenzionale, il bypass femoro-popliteo, distale, o disto-distale mentre anche a livello femoro-popliteo per le lesioni di tipo B e C i dati della letteratura di cui disponiamo non ci consentono di propendere per una piuttosto che per l’ altra opzione. Sempre più frequente è il ricorso, specie in pazienti che presentino più livelli di patologia, ad interventi ibridi (endovascolari + chirurgici convenzionali). In realtà il più delle volte le procedure endovascolari a livello dell’asse femoro-popliteo-distale presentano dei limiti in ragione del carattere particolarmente diffuso delle lesioni obliteranti e dell’esistenza di calcificazioni severe che rendono talora infruttuosi tali tentativi. Del resto l’iperplasia intimale e gli stress meccanici a livello dell’articolazione del ginocchio, ma anche delle masse muscolari della coscia, possono comprometterne i risultati a distanza anche a breve termine. E’ per tali motivi che una rivascolarizzazione chirurgica convenzionale conserva intatto il suo interesse. Nel contesto di un'ischemia critica diverse esperienze pubblicate in letteratura sembrerebbero però suggerire proprio in questa categoria di pazienti ad alto rischio sempre, quando possibile, un primo approccio endovascolare. Nel realizzare tali tentativi è però indispensabile preservare lo spazio per eventuali altre soluzioni chirurgiche che si rendessero necessarie in conseguenza di un insuccesso immediato o tardivo dell'angioplastica. Diverse sono le modalità di esecuzione di una rivascolarizzazione chirurgica, in funzione della scelta e della disponibilità del materiale che può essere una protesi, il più delle volte in PTFE, ovvero la safena interna, che può venire invertita, o lasciata “in situ”, previa soppressione dei giochi valvolari. Come già menzionato, le indicazioni al trattamento nelle rivascolarizzazioni distali devono essere piu’ rigorose, e nel caso di rivascolarizzazioni sotto-articolari vengono trattati solo pazienti in ischemia critica. In quest’ultimo caso le rivascolarizzazioni vengono eseguite preferenzialmente utilizzando la vena safena i cui risultati, secondo quattro casistiche della letteratura relative a un totale di circa 3000 pazienti, danno una pervietà primaria a 5 anni del 70%, una pervietà secondaria dell’81% e un «salvataggio» del 90% degli arti destinati altrimenti a un’amputazione. Di cruciale importanza è la sorveglianza eco-Doppler di tali bypass che consente di diagnosticare eventuali stenosi evolutive a livello delle arterie native prossimali o distali o a livello delle anastomosi, e quindi di correggerle con procedure endoluminali di PTA ovvero con procedure chirurgiche convenzionali, quali l’apposizione di un patch o l’interposizione di un corto innesto in vena. In caso di occlusione del bypass si può procedere o a una trombolisi percutanea ovvero a una trombectomia chirurgica o a un bypass iterativo.In conclusione gli elementi necessari per un progressivo miglioramento dei risultati nel trattamento dei pazienti affetti da arteriopatia cronica ostruttiva degli arti inferiori sono: · una profonda conoscenza della storia naturale della malattia e dell’associazione con altre localizzazioni, in particolare coronarica; · un'accurata valutazione clinica; · la correzione dei fattori di rischio, la terapia antiaggregante ed il trattamento riabilitativo, · un corretto impiego delle metodiche diagnostiche meno invasive, quali l’eco-Doppler e più recentemente l’angio-TAC e l’ Angio-Risonanza Magnetica che attualmente consentono di meglio definire le indicazioni a una rivascolarizzazione e soprattutto di adattare al singolo paziente la soluzione tecnica più adeguata.; · la valutazione del rischio chirurgico e l’adozione di misure, in particolare di protezione miocardica, rivolte a minimizzare tale rischio ; · un’attenta selezione ed una messa a punto di tecniche chirurgiche e/o endovascolari di rivascolarizzazione sempre più efficaci e durature; · un meticoloso follow-up dei pazienti affinché i risultati delle rivascolarizzazioni possano mantenersi a distanza.
BIBLIOGRAFIA ● Murad MH, Flynn DN, , Guyatt GH, Hobson RW 2nd, Erwin PJ, Montori VM Endarterectomy vs stenting for carotid artery stenosis: a systematic review and meta-analysis. J Vasc Surg. 2008 Aug;48(2):487-93 ● Brahmanandam S, Ding EL, Conte MS, Belkin M, Nguyen LL Clinical results of carotid artery stenting compared with carotid endarterectomy. J Vasc Surg. 2008 Jul;48(1):256-7. ● Hobson RW 2nd, Mackey WC, Ascher E, Murad MH, Calligaro KD, Comerota AJ, Montori VM, Eskandari MK, Massop DW, Bush RL, Lal BK, Perler BA; Society for Vascular Surgery. Management of atherosclerotic carotid artery disease: clinical practice guidelines of the Society for Vascular Surgery. J Vasc Surg. 2008 Aug;48(2):480-6 ● Ringleb PA, Chatellier G, Hacke W, Favre JP, Bartoli JM, Eckstein HH, Mas JL.Safety of endovascular treatment of carotid artery stenosis compared with surgical treatment: a meta-analysis. J Vasc Surg. 2008 Jul;48(1):256-7. ● Van der Vaart MG, Meerwaldt R, Reijnen MM, Tio RA, Zeebregts CJ. Endarterectomy or carotid artery stenting: the quest continues. Am J Surg. 2008 Feb;195(2):259-69 ● Cremonesi A, Setacci C, Bignamini A, Bolognese L, Briganti F, Di Sciascio G, Inzitari D, Lanza G, Lupattelli L, Mangiafico S, Pratesi C, Reimers B, Ricci S, de Donato G, Ugolotti U, Zaninelli A, Gensini GF. Carotid artery stenting: first consensus document of the ICCS-SPREAD Joint Committee. Stroke. 2007 Jul;38(7):e54. ● Rothwell PM .Medical and surgical management of symptomatic carotid stenosis. Int J Stroke. 2006 Aug;1(3):140-9 ● Naylor AR. Is surgery still generally the first choice intervention in patients with carotid artery disease? Surgeon. 2008 Feb;6(1):6-12. ● Lyden SP, Shimshak TM. Contemporary endovascular treatment for disease of the superficial femoral and popliteal arteries: an integrated device-based strategy. J Endovasc Ther. 2006 Feb;13 Suppl 2:II41-51. ● Norgren L, Hiatt WR, Dormandy JA, Nehler MR, Harris KA, Fowkes FG; TASC II Working Group. ● Inter-Society Consensus for the Management of Peripheral Arterial Disease (TASC II). J Vasc Surg. 2007 Jan;45 Suppl S:S5-67. ● Lantis J, Jensen M, Benvenisty A, Mendes D, Gendics C, Todd G. Outcomes of combined superficial femoral endovascular revascularization and popliteal to distal bypass for patients with tissue loss. Ann Vasc Surg. 2008 May-Jun;22(3):366-71. ● Hirsch AT, Haskal ZJ, Hertzer NR, Bakal CW, Creager MA, et al. ACC/AHA 2005 Practice Guidelines for the management of patients with peripheral arterial disease (lower extremity, renal, mesenteric, and abdominal aortic): a collaborative report from the American Association for Vascular Surgery/Society for Vascular Surgery, Society for Cardiovascular Angiography and Interventions, Society for Vascular Medicine and Biology, Society of Interventional Radiology, and the ACC/AHA Task Force on Practice Guidelines (Writing Committee to Develop Guidelines for the Management of Patients With Peripheral Arterial Disease): endorsed by the American Association of Cardiovascular and Pulmonary Rehabilitation; National Heart, Lung, and Blood Institute; Society for Vascular Nursing; TransAtlantic Inter-Society Consensus; and Vascular Disease Foundation. Circulation. 2006 Mar 21;113(11):e463-654 ● Iii EM, Giri J. Management of peripheral arterial disease patients: comparing the ACC/AHA and TASC-II guidelines. Curr Med Res Opin. 2008 Jul 28. ● Joels CS, York JW, Kalbaugh CA, Cull DL, Langan EM 3rd, Taylor SM Surgical implications of early failed endovascular intervention of the superficial femoral artery. J Vasc Surg. 2008 Mar;47(3):562-5. ● Fleisher LA, Beckman JA, Brown KA, Calkins H, Chaikof EL, Fleischmann KE, Freeman WK, Froehlich JB, Kasper EK, Kersten JR, Riegel B, Robb JF, Smith SC Jr, Jacobs AK, Adams CD, Anderson JL, Antman EM, Buller CE, Creager MA, Ettinger SM, Faxon DP, Fuster V, Halperin JL, Hiratzka LF, Hunt SA, Lytle BW, Nishimura R, Ornato JP, Page RL, Riegel B, Tarkington LG, Yancy CW; American College of Cardiology; American Heart Association Task Force on Practice Guidelines (writing Committee to Revise the 2002 Guidelines on Perioperative Cardiovascular Evaluation for Noncardiac Surgery); American Society of Echocardiography; American Society of Nuclear Cardiology; Heart Rhythm Society; Society of Cardiovascular Anesthesiologists; Society for Cardiovascular Angiography and Interventions; Society for Vascular Medicine and Biology; Society for Vascular Surgery. ACC/AHA 2007 guidelines on perioperative cardiovascular evaluation and care for noncardiac surgery: a report of the American College of Cardiology/American Heart Association Task Force on Practice Guidelines (Writing Committee to Revise the 2002 Guidelines on Perioperative Cardiovascular Evaluation for Noncardiac Surgery) developed in collaboration with the American Society of Echocardiography, American Society of Nuclear Cardiology, Heart Rhythm Society, Society of Cardiovascular Anesthesiologists, Society for Cardiovascular Angiography and Interventions, Society for Vascular Medicine and Biology, and Society for Vascular Surgery. J Am Coll Cardiol. 2007 Oct 23;50(17):e159-241. |