|
La valutazione del rischio nel paziente sottoposto a procedura di cardiologia interventistica ed a chirurgia cardiaca
Cesare Baldi S. C. di Cardiologia Dipartimento Medico-Chirurgico di Cardiologia A.O.” S. Giovanni di Dio e Ruggi d’Aragona” - SALERNO
Per il cardiologo interventista sta diventando sempre più comune affrontare condizioni estreme in cui viene chiamato ad effettuare procedure di interventistica coronarica (PCI) in pazienti che presentano una combinazione di problemi particolarmente seri, quali età avanzata, comorbidità multiple, instabilità emodinamica di grado avanzato o controindicazioni alla chirurgia coronarica. Come si regola, allo stato attuale, l’operatore? Nella maggioranza dei casi si orienta a spiegare al paziente i rischi connessi alla esecuzione (o, alternativamente, alla non esecuzione) della procedura allo scopo di ottenere un completo e consapevole consenso informato; ma può anche riservarsi il diritto di non essere lui ad effettuare la procedura e chiedere, eventualmente, il parere di un collega più esperto. In realtà bisogna chiedersi se esista una guida consolidata al delicato processo di presa di decisione in queste situazioni estreme. I cardiochirurghi sono da tempo abituati ad utilizzare nella loro abituale pratica clinica, ed in particolare nelle condizioni critiche, sistemi di valutazione a punti del rischio (Risk Scoring System- RSS) come il Parsonnet o l’EuroSCORE, allo scopo da supportare in maniera obbiettiva il processo decisionale. Le limitazioni nella accuratezza della predizione del rischio sono note per entrambi i sistemi; essi offrono, tuttavia, uno strumento comune e condiviso di definizione terminologica che garantisce un qualche grado di precisione nell’assistere il chirurgo, il paziente e la sua famiglia nel momento di prendere la difficile decisione di effettuare un intervento a cuore aperto. Esistono analoghi RSS per la PCI e, se esistono, come mai essi non sono correntemente utilizzati? Forse perché manca la determinazione (o l’incentivo) ad utililizzarli?
ü Come nasce un sistema di valutazione a punti del rischio? Nella seconda metà degli anni 90 sono stati sviluppati numerosi modelli statistici destinati a predire gli esiti avversi della PCI come la morte e le complicanze post-procedurali; ma, questi modelli , basati su tecniche di regressione logistica applicate ai fattori di rischio preprocedurali, non risultano di semplice applicazione e richiedono l’uso del computer, per la implementazione delle loro complesse formule. Per semplificare il processo di predizione del rischio, sono stati proposti dei sistemi di valutazione a punti (RSS) che prevedono la assegnazione ad ogni fattore di rischio di un determinato punteggio, proporzionato al peso intrinseco che quel fattore di rischio mostra all’interno del modello di regressione logistica dal quale il sistema deriva: la somma dei punti corrispondenti ai diversi fattori di rischio a cui è esposto il paziente candidato alla PCI totalizza il punteggio finale del rischio del paziente; ovviamente, ad ogni punteggio totale del rischio corrisponde un rischio atteso di esito avverso utilizzabile per orientare la decisione clinica finale. Nella fase iniziale di questo percorso metodologico, la maggior parte di questi RSS è stata sviluppata a partire dai database provenienti da singoli centri o da raggruppamenti comunque ristretti di più ospedali, cosa che inevitabilmente veniva a confinare la accuratezza della predizione del rischio alle popolazioni di pazienti da cui lo stesso RSS derivava. La ipotesi di lavoro che ha ispirato la progettazione degli RSS più robusti è stata innanzitutto di garantire una adeguata generalizzabilità dello strumento attraverso la derivazione da popolazione molto ampie e la necessità di validare il grado di precisione dello strumento, sia pure potente e affidabile all’interno della popolazione di provenienza, nell’ambito di una popolazione, altrettanto ampia e variegata, ma profondamente diversa. Queste considerazioni di ordine logico ci consentono di affrontare alcune spinose questioni di ordine statistico che vanno però conosciute, sia pure per grandi linee, per familiarizzare con le caratteristiche che un efficiente RSS deve possedere. Un buon sistema di valutazione a punti del rischio deve innanzitutto essere accurato, nel senso che deve evitare errori di sottostima o di sovrastima del rischio: se il rischio medio di sviluppare un evento all’interno di una popolazione è del 5%, allora si potrebbe essere accurati assegnando un rischio atteso del 5% ad ogni paziente, senza però garantire una adeguata precisione dal momento che si arriva ad assegnare la stessa prognosi a pazienti di differente profilo di rischio. Un buon RSS deve essere in possesso anche di una adeguata capacità discriminativa che correla con la precisione con cui risulta in grado di differenziare i pazienti a basso rischio da quelli ad alto rischio. La regressione logistica è il modello statistico standard che viene utilizzato per esprimere la probabilità a verificarsi di un evento come funzione lineare di una variabile indipendente (cioè il fattore di rischio); questo modello produce gli odds ratio come misura della associazione tra fattore di rischio ed evento. Alla costruzione del modello di regressione logistica concorreranno i fattori di rischio evidenti alla esperienza clinica senza alcun riferimento alla conoscenza della loro relazione con gli esiti del data set di partenza (generalmente viene raccomandato di esplorare un numero totale di fattori di rischio non > 10% di quelli presenti nel data set). La capacità discriminativa di un modello viene valutata attraverso la statistica c (c da concordanza), che, con l’impiego delle aree delle curve ROC, esprime la proporzione di volte in cui il modello riesce ad aggiudicare correttamente il rischio in una coppia di soggetti. Una volta che il modello finale è stato sviluppato, bisogna passare ad utilizzare il test di Hosmer-Lemeshow allo scopo di determinare se il modello riflette in maniera adeguata i dati osservati: il test consiste nel dividere tutto il campione in gruppi, in genere in decili, omogenei per valori attesi di rischio simili tra loro e, quindi, nel confrontare all’interno di questi gruppi i rapporti tra eventi attesi ed eventi osservati. Se il test verifica la globale concordanza tra eventi attesi ed eventi osservati, allora esso mostrerà una adeguata capacità di calibrazione. Alla fine, la configurazione definitiva del RSS incorporerà i diversi fattori di rischio, scelti in quanto associati in maniera significativa agli eventi osservati, come numeri interi che, sommati tra loro, realizzeranno un punteggio numerico che identifica la fascia di rischio di sviluppare eventi a cui appartiene il paziente; tutto ciò rende il lavoro del clinico molto più semplice senza sacrificarne la attendibilità perché il numero intero connesso al fattore di rischio esprime matematicamente, sia pure in maniera approssimata, il coefficiente dell’odds ratio ricavato dal modello di regressione logistica.
ü Quali sono i modelli di valutazione a punti del rischio in pazienti sottoposti a PCI? I modelli attualmente esistenti per la predizione del rischio di morte o di complicazioni dopo PCI sono numerosi, ma vanno ricordati solo i più rilevanti, perché costruiti con procedure che hanno rigorosamente rispettato le regole di metodologia statistica prima discusse: 1) New York (NY) State model, 2) American College of Cardiology–National Cardiovascular Data Registry (ACC-NCDR); 3) Northern New England (NNE); 4) Michigan Consortium; 5) William Beaumont Hospital; 6) Cleveland Clinic; 7) Mayo Clinic; 8) Brigham and Women’s Hospital. Tutti questi modelli sono stati sviluppati per predire la mortalità intraospedaliera e gli ultimi tre anche per predire il rischio di complicanze (IM, stroke e ricorso a BPAC). Le variabili inserite come fattori di rischio in tutti questi RSS appartengono in realtà a categorie ampie e ben note alla pratica clinica: § Età: l’età crescente rappresenta un importante fattore di rischio per le maggiori complicanze cardiovascolari in relazione alla ridotta riserva di funzione cardiaca, alla presenza frequente di malattia multivasale ed alla maggiore prevalenza di comorbidità; nel risk score della Mayo Clinic la probabilità di un ultratrottantenne a sviluppare complicanze è almeno sei volte superiore a quella di pazienti di età inferiore. Peraltro, la età avanzata rappresenta una probabilità incrementale di morte in tutti modelli, con un rischio atteso di almeno tre volte superiore in un ottuagenario rispetto ad un paziente in una fascia di età compresa tra i 50 e i 60 anni. § Funzione ventricolare sinistra: questo fattore viene incorporato nei diversi modelli di rischio con diversi parametri di valutazione; nel modello dello stato di NY, frazione di eiezione ridotta e scompenso cardiaco vengono considerati predittori indipendenti morte; nel modello della Mayo Clinic vengono presi in esame, ai fini della funzione VSin, i pazienti con classe NYHA =/ > 3, laddove nel modello NNE il valore di FE < 40% è in grado di identificare complicazioni. § Shock cardiogeno: si tratta del predittore più importante di complicanze postprocedurali: nei modelli della Cleveland Clinic e della Mayo Clinic valori di OR di complicanze intraospedaliere per i pazienti in shock oscillavano tra 12.7 e 4.95, rispettivamente. Il rischio di morte si aggirava tra il 28% nel modello ACC-NCDR ed il 33% nel modello del Michigan Consortium. § Presentazione in condizioni di emergenza: infarto miocardico acuto, arresto cardiaco ed instabilità emodinamica sono variabili che condizionano pesantemente l’esito della procedura; anche l’impiego della contropulsazone aortica nel corso di una procedura effettuata in urgenza costituisce un marcatore significativo del rischio di morte. § Caratteristiche angiografiche di alto rischio: malattia multivasale, malattia del tronco comune, presenza di trombo, lesione di tipo C, sec la classificazione ACC/AHA, non sono omogeneamente rappresentate in tutti i modelli di rischio. § Insufficienza renale: nonostante le differenti definizioni adottate per individuare la presenza prePCI di disfunzione renale, essa rimane un importante predittore di complicanze postprocedurali: nel modello del Michigan Consortium l’OR di mortalità nei pazienti candidati a PCI con una creatininemia > 1.5 mg/dl è pari a 5.5. § Vasculopatia periferica: si tratta di un fattore di rischio che identifica, se presente, un quadro di coronaropatia mediamente più avanzato sia in termini di severità che di diffusione delle lesioni: nel modello dello stato di NY l’OR per il rischio di morte nei pazienti con malattia dell’asse femoro-popliteo è pari a 1.77. Altri predittori ben noti, come il diabete mellito ed il sesso femminile, sono stati incorporati in alcuni modelli ma solo in una minoranza di essi, non riuscendo in quelli in cui non sono presenti a mostrare un peso prognostico sufficiente; altri predittori, che hanno sollevato un interesse epidemiologico per il loro impatto prognostico crescente , come la leucocitosi, la anemia e la presenza di marker infiammatori, non sono assolutamente contenuti nei correnti RSS.
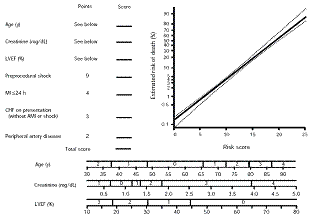
ü Quale modello scegliere nella pratica clinica? La performance di questi modelli, esaminati nella loro globalità, appare ancora pesantemente condizionata da numerose limitazioni: le variabili incluse nei differenti modelli sono state spesso incorporate con definizioni differenti ; la derivazione dei singoli modelli da database di istituzioni individuali o da consorzi ristretti di più istituzioni rappresenta un ostacolo concreto ad una ampia generalizzabilità dello strumento; in alcuni modelli esiti alternativi alla mortalità non sono stati calcolati; il volume di attività, espresso in termini di PTCA eseguite dal singolo operatore e dalla singola istituzione, non è stato testato; la classificazione ACC/AHA della gravità angiografica delle lesioni mostra una capacità discriminativa modesta; gli eventi a bassa incidenza richiederebbero la estrazione dei dati da parte di dataset più ampi; gli intervalli di tempo, spesso troppo estesi, tra la acquisizione dei dati e la costruzione del modello rappresentano un forte ostacolo alla reale applicabilità del modello alla pratica clinica corrente; i criteri più recenti di definizione di infarto miocardico non sono disponibili. Tutti questi modelli, cionondimeno, mostrano una capacità discriminativa con la statistica c che va dal valore di 0.782 nel modello della Mayo Clinic a quello di 0.892 nel modello dello stato di NY, anche se i modelli che predicono il rischio di morte appaiono generalmente più robusti dei modelli che predicono il rischio di complicanze postprocedurali. La previsione della probabilità di un evento non può essere assimilata alla lettura nitida del futuro nella sfera di cristallo: la maggioranza dei pazienti ad alto rischio verosimilmente non svilupperà alcuna complicanza nel senso che il vero obbiettivo di un modello di rischio consiste nello stratificare correttamente i pazienti in categorie di rischio basso, moderato ed elevato. In altri termini, un modello di rischio efficiente è in grado di predire gli eventi avversi postprocedurali nella media dei pazienti, ma non è costruito per definire con assoluta precisione il rischio del singolo paziente; inoltre il paziente singolo può presentare altri problemi medici rilevanti ma epidemiologicamente marginali che non sono stati incorporati nel modello di rischio (si pensi al coma postanossico successivo ad un arresto cardiaco prolungato o alla diagnosi recente di leucemia). In definitiva, uno score di rischio dovrebbe essere utilizzato per guidare il cardiologo ed il paziente a prendere una decisione consapevole e non a prevedere in anticipo l’esito specifico del singolo paziente. Tenendo in mente tutte queste considerazioni, appare legittimo selezionare nella moltitudine dei RSS disponibili , i due risk score che sembrano mostrare i requisiti di maggiore efficienza: il New York risk score e il Mayo Clinic risk score. Il primo è stato costruito su un data set consistente che si riferisce ad un numero totale elevatissimo di variabili connesse ad oltre 45000 PCI effettuate in 46 ospedali diversi dello stato di New York nel 2002; il modello di regressione logistica ha considerato numerosi fattori di rischio dei quali solo nove sono entrati nel sistema di valutazione con pesi variabili da 1 a 9 e con punteggio totale di rischio (inteso come somma dei punteggi individuali di ognuna delle nove variabili) oscillante tra 0 e 40. I punteggi assegnati alla variabile età sono 1 per la fascia di età compresa tra 56 e 64 anni, 3 per la fascia tra 65 e 74 anni ed infine 5 sopra i 75 anni; lo shock cardiogeno totalizza da solo 5 punti; l’infarto miocardico realizza un punteggio di 2 se la PCI viene effettuata al di là dei 14 giorni dall’evento, e un punteggio pari a 9 nel casi di procedura effettuata entro le 24 ore a partire da una occlusione trombotica di stent. Nel 2007 Singh e coll hanno messo a punto un modello di rischio innovativo tenendo presente alcuni problemi ancora evidenti nei modelli di rischio correntemente utilizzati ed in particolare: la impossibilità di utilizzare, per la stratificazione prima della procedura, i modelli correnti a causa della necessità di conoscere alcune variabili angiografiche incorporate in esso; la restrizione di alcuni modelli alla predizione del rischio di morte e non del rischio di complicanze; l’impiego di variabili definite sulla base di giudizi soggettivi e non di valutazioni quantitative. Il nuovo modello di rischio della Mayo Clinic è stato pertanto progettato con il dichiarato obbiettivo di poter disporre nella pratica quotidiana di uno strumento aggiornato in grado di definire il rischio prima della esecuzione della procedura sulla base di dati di natura esclusivamente clinica e non invasiva. Un esempio della modalità di calcolo dello score di rischio di morte è rappresentato nella fig 1 nella quale compaiono 7 variabili, 3 continue a cui assegnare un punteggio determinabile con l’aiuto del nomogramma, e 4 categoriche con punteggio preassegnato da aggiungere alla somma finale se presenti nel paziente in esame.
Fig1: Modello di rischio della Mayo Clinic per la predizione della morte intraospedaliera (estratto da Singh M: Bedside estimation of risk from PCI - Mayo Clin Proc 2007;82:701-708)
Recentemente la potenza predittiva del Mayo Clinic risk score è stata confermata attraverso un processo di validazione esterna grazie al quale esso è stato applicato in un popolazione diversa da quella da cui è stato derivato e di proporzioni molto più ampie, il National Cardiovascular Data Registry contenente i dati relativi alle procedure effettuate in 309.351 pazienti tra il 2004 e il 2006; il modello Mayo ricalibrato dopo il processo di validazione ha mostrato una capacità discriminativa eccellente a conferma della possibilità di utilizzo di uno strumento predittivo in fase preprocedurale, basato su variabili cliniche e non angiografiche o intraprocedurali, che potrebbe rappresentare la piattaforma di dialogo oggettivo nel colloquio con il paziente e con i suoi familiari e venire quindi incorporato nel processo di acquisizione del consenso informato.
ü A cosa serve la implementazione di un modello per la predizione del rischio connesso a PCI? Perché non siamo già in grado di effettuare una valutazione formale del rischio connesso a PCI? Forse perché siamo pigri, o perché siamo soddisfatti dei nostri risultati, o, ancora, perché riteniamo che si tratti di strumenti troppo complessi per poter essere applicati nella pratica clinica? La verità è che esistono ormai delle forti pressioni che si ribaltano sul cardiologo interventista: basti pensare alla recente pubblicazione sui giornali, non solo statunitensi ma anche britannici, dei dati relativi alla mortalità dei singoli cardiochirurghi in un trend che verosimilmente si allargherà dall’ area della chirurgia cardiaca a quella della interventistica coronarica. In questa prospettiva il risk score può diventare uno strumento di autotutela del cardiologo interventista ed essere utilizzato sia per neutralizzare l’impatto dei casi di maggiore complessità ( e con tassi di maggiore mortalità) negli ospedali terziari, che altrimenti rimarrebbero penalizzati sotto il peso di risultati apparentemente inferiori se non interpretati alla luce del più alto profilo di rischio dei pazienti, sia per documentare che i rischi di una procedura potenzialmente complessa sono stati discussi preliminarmente con il paziente. ü I problemi connessi con l’impiego dei sistemi di valutazione del rischio in chirurgia cardiaca L’utilizzo di un sistema per la stratificazione del rischio chirurgico rappresenta un utile strumento per uniformare la valutazione dei pazienti, basato non su impressioni cliniche soggettive ma su parametri condivisi e misurabili. Questo consente di fornire, al paziente, un’adeguata informazione sul rischio chirurgico attraverso il confronto oggettivo dei dati di casistiche diverse, e, al singolo centro, di verificare se i risultati ottenuti al proprio interno rientrino nei valori di riferimento. Nelle ultime due decadi sono stati sviluppati numerosi RSS applicati alla chirurgia cardiaca; il primo modello di predizione del rischio è stato il Parsonnet score, utilizzato sia dalle istituzioni ospedaliere che dai singoli operatori per confrontare con un benchmark gli esiti della attività chirurgica aggiustata per il profilo di rischio dei pazienti operati, ma esso mostrò un significativo difetto di sovrastima della mortalità . Successivamente, nel 1999, fu introdotto l’EuroSCORE additivo, che assegna un punteggio espresso in numeri interi ad ognuno dei 17 fattori di rischio identificati come predittori di mortalità operatoria per andare a totalizzare un punteggio finale che identifica il rischio previsto di morte intraospedaliera. Questo modello è stato sottoposto a numerose validazioni, anche all’esterno della comunità dei cardiochirurghi europei da cui il modello stesso è stato derivato, in particolare negli Stati Uniti ed in Australia: esso ha mostrato, nella popolazione globale dei pazienti candidati a chirurgia coronarica ed a chirurgia valvolare, una ragionevole capacità predittiva complessiva dei risultati, denunciando però, nelle procedure coronariche, una sostanziale sovrastima del rischio atteso rispetto al rischio realmente osservato; inoltre la capacità predittiva è risultata scadente nel sottogruppo dei pazienti ad alto rischio mentre la mortalità della chirurgia di combinazione valvolare e coronarica è risultata sottostimata. Più recentemente, a partire dagli stessi fattori di rischio ma con un algoritmo più complesso che richiede l’uso del computer per la introduzione diretta dei coefficienti derivati dalla regressione logistica che è alla base del modello, è stata disegnata una configurazione innovativa di questo modello, l’EuroSCORE logistico, a cui è stato attribuito un potere predittivo della mortalità operatoria più elevato di quello dell’EuroSCORE additivo. Effettivamente esso sembra comportarsi meglio nella fascia dei pazienti ad alto rischio, ma indagini di validazione effettuate in diversi contesti istituzionali ne hanno nuovamente sottolineato il sostanziale difetto di sovrastima del rischio e ne hanno suggerito una ricalibrazione nelle singole istituzioni e nelle singole fasce di rischio in cui venga utilizzato. Allo stato attuale, nonostante la diffusione di un numero elevato di RSS in chirurgia cardiaca e la notevole esperienza accumulata con alcuni di essi, rimane difficile stratificare il rischio del singolo paziente, soprattutto di quello ad alto rischio; tutto ciò probabilmente continuerà ad avere un impatto di rilevante, e disturbante, incertezza, nella pratica clinica comune nella quale sempre più spesso, in relazione ai promettenti risultati della Cardiologia Interventistica nel trattamento percutaneo della stenosi aortica critica o della malattia del tronco comune, saremo chiamati a prendere in considerazione, nel paziente ad altissimo rischio chirurgico, una opzione terapeutica alternativa a quella chirurgica tradizionale. BIBLIOGRAFIA ESSENZIALE
1. Kimmel SE, Berlin JA, Strom BL, et al. Development and validation of simplified predictive index for major complications in contemporary percutaneous transluminal coronary angioplasty practice: the Registry Committee of the Society for Cardiac Angiography and Interventions. J Am Coll Cardiol. 1995;26:931–938. 2. Moscucci M, Kline-Rogers E, Share D, et al. Simple bedside additive tool for prediction of in-hospital mortality after percutaneous coronary interventions. Circulation. 2001;104:263–268. 3. O’Connor GT, Malenka DJ, Quinton H, et al. Multivariate prediction of in-hospital mortality after percutaneous coronary interventions in 1994-1996: Northern New England Cardiovascular Disease Study Group. J Am Coll Cardiol. 1999;34:681– 691. 4. Qureshi MA, Safian RD, Grines CL, et al. Simplified scoring system for predicting mortality after percutaneous coronary intervention. J Am Coll Cardiol. 2003;42:1890 –1895. 5. Resnic FS, Ohno-Machado L, Selwyn A, et al. Simplified risk score models accurately predict the risk of major in-hospital complications following percutaneous coronary intervention. Am J Cardiol. 2001;88:5–9.. 6. Singh M, Lennon RJ, Holmes DR Jr, et al. Correlates of procedural complications and a simple integer risk score for percutaneous coronary intervention. J Am Coll Cardiol. 2002;40:387–393. 7. Wu C, Hannan EL, Walford G, et al. A risk score to predict in-hospital mortality for percutaneous coronary interventions. J Am Coll Cardiol. 2006;47:654–660. 8. Singh M, Rihal CS, Selzer F, et al. Validation of Mayo Clinic risk adjustment model for in-hospital complications after percutaneous coronary interventions, using the National Heart, Lung, and Blood Institute dynamic registry. J Am Coll Cardiol. 2003;42:1722–1728. 9. Singh M, Rihal CS, Lennon RJ, et al. Comparison of Mayo Clinic Risk Score and American College of Cardiology/American Heart Association lesion classification in the prediction of adverse cardiovascular outcome following percutaneous coronary interventions. J Am Coll Cardiol. 2004;44:357–361. 10. O’Connor GT, Malenka DJ, Quinton H, et al. Multivariate prediction of in-hospital mortality after percutaneous coronary interventions in 1994-1996. Northern New England Cardiovascular Disease Study Group. J Am Coll Cardiol 1999;34:681 - 91. 11. Moscucci M, Kline-Rogers E, Share D, et al. Simple bedside additive tool for prediction of in-hospital mortality after percutaneous coronary interventions. Circulation 2001;104:263 -8 12. Roques F, Nashef SA, Michel P, et al. Risk factors and outcome in European cardia surgery: analysis of the EuroSCORE multinational database of 19,030 patients. Eur J Cardiothorac Surg 1999;15:816–23. 13. Karthik S, Srinivasan AK, Grayson AD, et al. Limitations of additive EuroSCORE for measuring risk stratified mortality in combined coronary and valve surgery. Eur J Cardiothorac Surg 2004;26:318–22. 14. Gogbashian A, Sedraykan A, Treasure T. EuroSCORE: a systematic review of international performance. Eur J Cardiothorac Surg 2004;25:695–700. 15. Roques F, Michel P, Goldstone AR, et al. The logistic EuroSCORE. Eur Heart J 2003;24:1–2. 16. Michel P, Roques F, Nashef SA, et al. Logistic or additive EuroSCORE for high risk patients? Eur J Cardiothorac Surg 2003;23:684–7. |