|
Lo Scompenso Cardiaco oggi
Domenico Miceli, Eleonora De Luca, Armando Maria Scalzone, Pio Caso, Raffaele Calabrò UOS Valutazione dello Scompenso Cardiaco e Riabilitazione Cardiologica Dipartimento di Cardiologia AO Monaldi, Napoli
Negli ultimi venti anni abbiamo assistito ad un profondo mutamento delle conoscenze in tema di fisiopatologia dello Scompenso Cardiaco (SC): da un modello concettuale puramente emodinamico che riconosceva nella riduzione della contrattilità miocardica il perno fondamentale della sindrome, ad un modello neuro-ormonale coinvolgente i meccanismi regolatori che ruotano attorno al sistema adrenergico e all’asse renina-angiotensina-aldosterone, fino al modello neuro-umorale rappresentato dallo studio delle variazioni degli ormoni ANP e BNP e dei loro metaboliti (fig.1).
Figura 1
Tutto ciò, come è noto, ha provocato rilevanti conseguenze dal punto di vista terapeutico: trenta anni fa sarebbe stato contro ogni logica trattare un paziente affetto da SC con un betabloccante, mentre oggi può addirittura essere considerato non eticamente corretto privare un simile paziente di questa categoria di farmaci. Nel frattempo, però, lo SC si sta rivelando una sindrome in costante aumento : il flusso informativo derivante dalle Schede di Dimissione Ospedaliera del 2003 (1) segnala 197.818 dimissioni con il DRG 127 (Scompenso Cardiaco e Shock), con un trend in crescita rispetto ai 175.470 ricoveri del 1999, e con un costo ospedaliero globale, ottenuto aggiungendo il DRG 103 (Trapianto Cardiaco), di 500 miliardi di euro. L’incidenza annuale viene stimata approssimativamente intorno a 300 nuovi casi ogni 100.000 persone, ma è previsto che il numero possa raddoppiare nei prossimi 40 anni a causa dell’invecchiamento della popolazione. La dimensione del fenomeno, soprattutto dal punto di vista delle ricadute cliniche, è confermata dagli studi osservazionali condotti in ambito ospedaliero, e, tra questi, dai dati del TEMISTOCLE ( hearT failurE epideMIological STudy fadOi – anmCo in italian peopLE )(2), uno studio osservazionale condotto in collaborazione tra l’Associazione Nazionale Medici Cardiologi Ospedalieri(ANMCO) e la Federazione delle Associazioni dei Dirigenti Ospedalieri Internisti(FADOI), che ha “fotografato” per 12 giorni dell’anno 2000 il percorso ospedaliero di 2127 pazienti con SC in 167 UO di Cardiologia e 250 UO di Medicina italiane. Lo studio TEMISTOCLE ha dimostrato che : · i pazienti con SC hanno una ridotta quantità e qualità di vita: Ø il 5% muore in ospedale Ø il 15% muore entro sei mesi dalla dimissione Ø il 45% ritorna in ospedale almeno una volta entro sei mesi dalla dimissione
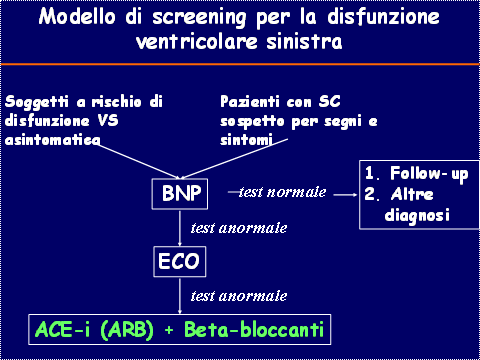
Come sostenuto in un’ analisi di Cleland (3), il carico gestionale totale dello SC risulta essere il 5% della popolazione generale, e questo valore percentuale risulta composto da : · 1% SC con manifestazioni di disfunzione sistolica ventricolare sinistra (1,5% per età comprese fra 25 e 75 anni) · 1% SC con disfunzione ventricolare sinistra asintomatica · 1% SC con funzione sistolica conservata · 2% SC sospetto ma non confermato Ciò farebbe stimare che, in Italia, vi siano circa 3.000.000 di cittadini affetti da SC sia in forma asintomatica che conclamata: infatti la revisione 2005 delle Linee Guida per la diagnosi e la terapia dello SC cronico (4), sottolinea l’importanza di sviluppare strategie terapeutiche di medio e lungo termine volte ad impedire lo sviluppo e la progressione del danno cardiaco e della disfunzione ventricolare sinistra asintomatica verso lo SC clinicamente manifesto, nella convinzione, come desunto dai risultati degli studi di comunità (5,6), che quando lo SC si manifesta clinicamente la prognosi è molto severa, e presenta una involuzione paragonabile a quella delle più gravi forme di cancro (7). La prevenzione primaria dello SC, quindi, suggerisce ed anzi impone di trattare con aggressività i principali fattori di rischio per SC, ovvero la cardiopatia ischemica in primo luogo, ma anche l’ ipertensione arteriosa e il diabete mellito, e pertanto coinvolge ad ampio raggio la prevenzione cardiovascolare in senso lato, rivolta alla correzione degli stili di vita scorretti con messaggi destinati alla popolazione generale, con l’aiuto di tutte le figure professionali della Sanità pubblica e Privata, dai Medici di Medicina Generale agli Specialisti Territoriali, ai Medici Ospedalieri e agli Infermieri. A questo scopo la comunità scientifica, ed in particolare l’ANMCO, è impegnata a proporre un modello di screening da diffondere mediante sperimentazioni nazionali su larga scala attraverso l’utilizzo di un algoritmo per l’identificazione della disfunzione ventricolare sinistra asintomatica simile a quello proposto dalle Linee Guida ESC 2005 per i pazienti sintomatici, che prevede l’utilizzo dei peptidi natriuretici anche per limitare il numero di ecocardiogrammi necessari per la diagnosi di nuovi casi di disfunzione ventricolare risparmiando così risorse (fig.2).
Figura 2
Ma accanto alle più che opportune misure di prevenzione primaria, la battaglia contro l’”epidemia” SC va condotta anche sul fronte della prevenzione secondaria, allo scopo di ridurne in primo luogo la mortalità ma anche la morbidità che, considerate le frequenti instabilizzazioni della malattia, inducono un frequente ricorso alla ospedalizzazione e soprattutto alla riospedalizzazione. Sotto questo aspetto il nostro armamentario terapeutico si è arricchito, in questi ultimi anni, di diverse categorie di farmaci la cui efficacia è ormai ampiamente dimostrata dalle evidenze degli studi clinici controllati e randomizzati: l’approccio terapeutico si è infatti adattato, nel corso del tempo, alle modifiche concettuali che via via hanno caratterizzato la comprensione delle basi fisiopatologiche dello SC. Farmaci come gli ACE-inibitori e i betabloccanti, ma anche, come sottolineato nelle ultime Linee Guida ESC già citate, i sartani, hanno mostrato consistenti riduzioni percentuali di mortalità e ospedalizzazione per SC, purchè utilizzati il più precocemente possibile e soprattutto al meglio delle dosi raccomandate. Difatti, uno dei problemi più attuali in tema di SC è oggi rappresentato proprio dal sottoutilizzo di questi farmaci: dallo studio SHAPE(8), la più vasta indagine sullo SC condotta in Europa che ha promosso, attraverso l’ANMCO e l’Heart Care Foundation nel novembre 2005, la Settimana Europea dello Scompenso Cardiaco, è emerso che in più del 50% dei casi il Medico di Medicina Generale europeo non prescrive al paziente la terapia ottimale: solo poco più di 1 su 2 prescrive gli ACE-inibitori come trattamento di prima scelta e solo 1 su 3 aggiunge alla terapia il betabloccante, mentre solo il 64% degli Internisti e dei Geriatri e solo l’82% dei Cardiologi prescrive queste classi di farmaci. Nel frattempo piuttosto deludenti sono stati i risultati ottenuti dai trial che hanno testato nuovi trattamenti, come gli antagonisti dell’endotelina, del TNF-alfa o delle endopeptidasi neutre, generando anzi la convinzione che si sia raggiunto ormai il limite della potenzialità della terapia neuroormonale. E, mentre la terapia con le cellule staminali è ancora da considerarsi una prospettiva futura a tutt’oggi sperimentale, nuove speranze per i malati di SC grave arrivano dalla cardiochirurgia e dall’impianto di nuovi presidi: le alternative chirurgiche innovative prevedono, tra l’altro, l’applicazione di un ventricolo artificiale nella gabbia toracica, una soluzione potenzialmente utile come ponte verso un trapianto di cuore o come decisione definitiva in quei malati in cui il trapianto non è indicato, ad esempio perché troppo anziani; anche in questo campo le novità, naturalmente per pazienti selezionati, non mancano, e sono principalmente rappresentate dai ventricoli artificiali di piccole dimensioni che possono essere impiantati indipendentemente dalla superficie corporea del paziente. Per quanto riguarda i nuovi presidi, è ormai noto che la terapia di resincronizzazione cardiaca (CRT), associata alla terapia medica dello SC, ha dimostrato di ridurre il rischio di morte per scompenso fino al 45% e fino al 53% di morte cardiaca improvvisa, come dimostrato dai risultati dello studio CARE HF (CArdiac REsynchronization in Heart Failure) (9). E i dati precedenti dello studio COMPANION(10) e dello studio SCD-HeFT(11), suggeriscono, in questi pazienti, indipendentemente dall’eziologia dello SC, l’impianto del pacemaker biventricolare con funzione di defibrillatore, anche se, nelle indicazioni all’applicazione di questi dispositivi, sussiste tuttora qualche controversia in merito alla definizione di più precisi criteri di selezione dei pazienti che possono trarne il massimo beneficio garantendo un appropriato utilizzo delle risorse economiche : è possibile che, in futuro, anche con l’apporto delle nuove tecnologie ecocardiografiche, in particolare del DTI (Doppler Tissue Imaging), si possano individuare ulteriori più specifici parametri di indicazione nella selezione dei pazienti. Infine, è da poco disponibile un dispositivo per il monitoraggio dell’acqua intracorporea in pazienti scompensati: mediante l’OptiVol Fluid Status Monitoring (12) si possono misurare le variazioni di impedenza intratoracica, che costituiscono un’indicazione delle variazioni del volume ematico. La capacità di monitorare lo stato dei liquidi consente di correggere preventivamente la terapia prima che si inneschi la cascata emodinamica e neuroormonale che conduce all’instabilizzazione del compenso clinico. Ultimo, ma di certo non in ordine di importanza, è il problema dell’organizzazione dell’assistenza di questi pazienti, soprattutto in relazione alla continuità tra ospedale e territorio: il paziente con SC, come sovente accade nelle malattie croniche caratterizzate da fasi di stabilità/instabilità, ha necessità di particolari strategie e percorsi assistenziali in relazione alla diversa diagnosi eziologica, severità clinica e coesistenza di patologie associate, con il concorso di tutte le figure professionali a tutti i livelli. Questa, insieme con la soluzione dei quesiti ancora aperti in tema di terapia elettrica, il perfezionamento dei devices e la scoperta di nuovi farmaci da affiancare a quelli ormai già collaudati ma purtroppo non ancora implementati in maniera ottimale, rappresenta la chiave in grado di fornire ai pazienti con SC migliori prospettive di qualità e quantità di vita.
BIBLIOGRAFIA
1) Ministero della Salute. Dipartimento della Programmazione ( http://www.ministerosalute.it/programmazione/sdo/sdo.jsp ) 2) Di Lenarda A, Scherillo M, Maggioni AP et Al. Current presentation and management of heart failure in cardiology and internal medicine hospital units:a tale of two worlds. The TEMISTOCLE study. Am Heart J 2003;146:e12 3) Cleland JGF,Khand A,Clark A . The heart failure epidemic:exactly how big is it? Eur Heart J 2001;22:623-626 4) Cleland J, Dargie H, Drexler H et Al. Task Force for the Diagnosis and Treatment of Chronic Heart Failure of the European Society of Cardiology, Guidelines for the diagnosis and treatment of chronic heart failure. Eur Heart J, 2005; 26: 1115-1140 5) He J, Ogden LG, Bazzano LA et Al. Risk factors for congestive heart failure in US men and women: NAHNES I epidemiologic follow-up study. Arch Intern Med 2001;161:996-1002 6) Lloyd-Jones DM, Larson MG, Leip EP et Al. for the Framingham Heart Study. Lifetime risk for developing congestive heart failure: the Framingham Heart Study. Circulation 2002;106:3068-72 7) Stewart S, MacIntyre K, Hole DJ et Al. More “malignant” than cancer? Five-year survival following a first admission for heart failure. Eur J Heart Fail 2001;3:315-22 8) Remme WJ, McMurray JJV, Rauch B et Al. Public awareness of heart failure in Europe: first results from SHAPE. Eur Heart J, 2005;26:2413-2421 9) Cleland JG, Daubert JC, Erdmann E et Al. Long-term effects of cardiac resynchronization therapy on mortality in heart failure (the Care HF trial extension phase) Eur Heart J 2006; 27:1928-32 10) Bristow MR, Saxon LA, Bohemer J et Al. Cardiac-resynchronization with or without an implantable defibrillator in advanced chronic heart failure. New Engl J Med 2004;350:2140-50 11) Bardy GH, Lee KL, Mark DB et Al. Amiodarone or an implantable cardioverter-defibrillator for congestive heart failure N Engl J Med 2005;352:225-37 12) Adamson PB, Magalski A, Braunschweig F et Al. Ongoing right ventricular hemodynamics in heart failure: clinical value of measurements derived from an implantable monitoring systems J Am Coll Cardiol 2003;41:565-571
|