I
FARMACI ANTIARITMICI OGGI: USI E ABUSI
Jorge
Salerno-Uriarte
Dipartimento di Scienze Cardiovascolari. Università degli
Studi dell’Insubria. Ospedale di Circolo e Fondazione
Macchi, Varese.
I farmaci antiaritmici sono sempre stati molto impiegati nel
trattamento delle aritmie cardiache data la loro capacità
di modificare le caratteristiche elettrofisiologiche delle cellule
miocardiche sia agendo direttamente che indirettamente sul substrato
anatomico responsabile dell’aritmia senza tuttavia modificarlo
in maniera risolutiva e non garantendo quindi un effetto veramente
“curativo” dell’aritmia stessa. I farmaci
antiaritmici, in rapporto alle caratteristiche delle singole
aritmie e alla biodisponibilità e farmacocinetica della
singola molecola antiaritmica, potranno essere utilizzati sempre
più appropriatamente in rapporto alle conoscenze dell’utilizzatore.
Per il corretto impiego della terapia farmacologia sarà
necessario non solo conoscere a fondo il meccanismo d’azione
dei farmaci impiegati ma sopratutto il loro preciso effetto
in quel dato contesto clinico. La presenza o meno di cardiopatia
è fondamentalente nel tipo di risposta alla terapia farmacologica
e la sua scelta è condizionata da tale fattore in maniera
determinante..
Nella figura 1 viene raffigurata in maniera molto semplice,
con un rettangolo e una diagonale, quella che è l’incidenza
di una tale aritmia (di tipo sopraventricolare o ventricolare)
in presenza a meno di una cardiopatia
I
farmaci antiaritmici e loro inquadramento classificativi
Due ben note classificazioni dai farmaci antiaritmici hanno
cercato, in due tempi successivi, di caratterizzare e raggruppare
tali farmaci a seconda del loro meccanismo d’azione. La
classificazione dei farmaci antiaritmici proposta da Vaugham
Williams 1 e successivamente modificata da Harrison 2 è
riportata in tabella: Questa classificazione schematica suddivide
i farmaci in base al loro meccanismo d’azione. La Tabella
1 riporta, assieme alla classificazione per classi e alla descrizione
del meccanismo d’azione, le modificazioni indotte sull’elettrocardiogramma
di superficie e i nomi dei principali farmaci antiaritmici appartenenti
alla classe. Questa classificazione schematica suddivide i farmaci
in base al loro meccanismo d’azione. Riporta inoltre le
modificazioni indotte sull’elettrocardiogramma di superficie
e i nomi dei principali farmaci antiaritmici appartenenti alla
classe. Come si può notare, la Classe I comprende i farmaci
che bloccano i canali rapidi del sodio, le Classi II e IV comprendono
rispettivamente i farmaci beta-bloccanti e calcio-antagonisti,
mentre la Classe III i farmaci che esercitano un’azione
antiaritmica prolungando la durata del potenziale d’azione
e pertanto la refrattarietà. La Classe I a sua volta
si divide in tre sottoclassi (A, B e C) a seconda della diversa
azione sulla fase 0 del potenziale d’azione, sulla conduzione
e sulla ripolarizzazione.

Figura
1
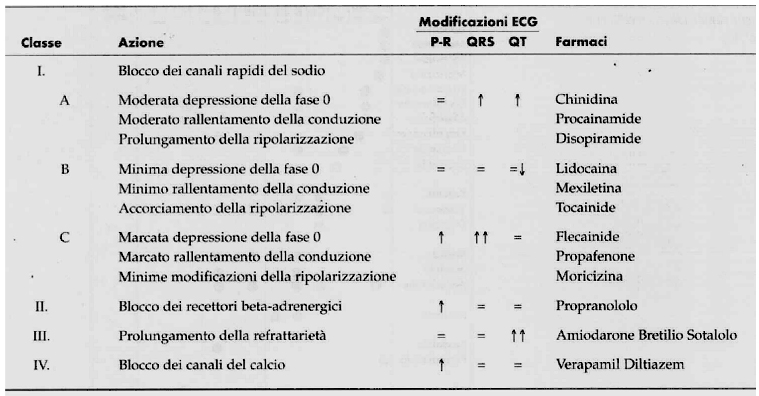
Tabella I
Figura
2
Questa classificazione sebbene sia largamente utilizzata in
un ampio contesto di caratterizzazione di un farmaco antiaritmico,
presenta molte limitazioni. Prima di tutto, il meccanismo d’azione
dei farmaci in questa classificazione viene valutato su tessuto
miocardico sano, specialmente su fibre di Purkinje, mentre molto
spesso le aritmie cardiache si associano ad una cardiopatia
organica che modifica in modo importante la struttura e la funzione
del tessuto miocardico. Inoltre, proprio perché i canali
ionici possono avere una struttura molecolare molto simile tra
loro, il meccanismo d’azione di alcuni farmaci è
in realtà il risultato della loro interazione su più
di un canale ionico. Basti pensare alla chinidina, che blocca
sia i canali del sodio sia quelli del potassio, oppure all’amiodarone,
la cui azione spazia per tutte e quattro le Classi. Inoltre,
questa classificazione non tiene in considerazione alcune variabili,
come la presenza di squilibri elettrolitici, i valori di pH,
la frequenza cardiaca e le variazioni del tono neurovegetativo,
che in clinica possono avere un ruolo determinante per l’effetto
che un determinato farmaco ottiene.
Un successivo tentativo di classificazione dei farmaci antiaritmici
è rappresentato dal “Sicilian Gambit” 3,
il cui nome origina da gambit, termine inglese per indicare
una mossa di scacchi con cui si sacrifica un pezzo per ottenere
un vantaggio e dal fatto che gli autori si riunirono a Taormina
per redigere questa classificazione, pubblicata nel 1991. Essi
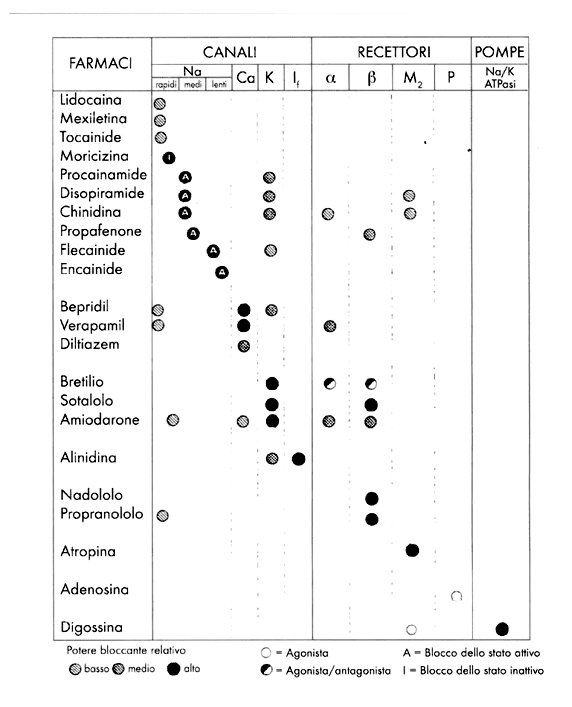
compilarono, sulla base di una revisione dell’attività
dei canali ionici, uno schema (Figura 2) in cui viene riassunto
per ogni singolo agente il profilo della sua azione sui canali
ionici, sui recettori e sulla pompa Na+/K+. L’uso di vari
simboli è utilizzato per indicare la potenza relativa
(bassa, moderata ed alta) dell’agente, il suo effetto
agonista o antagonista sul recettore ed il blocco dello stato
attivo o inattivo del canale ionico. Come corollario di questa
classificazione e sulla base di una revisione dei meccanismi
aritmogenetici, venivano anche evidenziati i farmaci antiaritmici
in grado di agire sui parametri vulnerabili di una determinata
aritmia cardiaca. Questa classificazione è un’eccellente
revisione dei meccanismi elettrofisiologici di base e dei possibili
meccanismi d’azione dei farmaci antiaritmici sull’aritmogenesi.
Va sottolineata infatti la capacità di riassumere il
profilo antiaritmico anche qualora questo si prospetti complesso
come nei casi dell’amiodarone, della chinidina, del verapamil
o del sotalolo. Tuttavia, a quasi quindici anni dalla sua introduzione,
questa classificazione è scarsamente utilizzata sia dal
cardiologo clinico sia dal farmacologo, che spesso fanno riferimento
alla precedente classificazione. Inoltre nell’impiego
clinico, diversi farmaci antiaritmici possono essere utilizzati
efficacemente per trattare la stessa aritmia, anche se hanno
meccanismi ionici completamente diversi, in quanto la complessità
delle situazioni osservate nelle aritmie cliniche consente di
agire su differenti variabili per terminarla. Basti pensare
infatti all’utilizzo del verapamil o della flecainide
per cessare una tachicardia da rientro ortodromico lungo una
via accessoria atrioventricolare: questi due farmaci sono infatti
in grado di terminare l’aritmia anche se con meccanismi
che agiscono su due punti critici completamente diversi del
circuito di rientro come, rispettivamente, il nodo atrioventricolare
e la via accessoria.
La
terapia farmacologia antiaritmica oggi
La terapia farmacologica delle aritmie cardiache è molto
mutata negli ultimi anni in particolare nell’era del dopo-CAST
(Cardiac Arrhythmias Suppression Trial). 4,5 Tutte le linee
guida concernenti il trattamento delle aritmie ventricolari
post infartuali potenzialmente letali sono pesantemente condizionate
dalle informazioni emerse a seguito della diffusione dei risultati
dello studio CAST. 6,7 Lo sviluppo tecnologico avvenuto nell’ultimo
ventennio ha certamente favorito in maniera determinante lo
sviluppo del defibrillatore automatico impiantabile 8 il quale,
dotato o meno di funzione di pacing antitachicardico, è
diventato un presidio sempre più sofisticato negli ultimi
tempi rivoluzionando il trattamento delle aritmie maligne. Un
altro elemento è stato determinante fin dalla fine degli
anni ’80 nell’impedire gli abusi della terapia farmacologia
e favorendo l’uso più appropriato dei farmaci antiaritmici;
ci riferiamo in particolare all’avvento della trattamento
non farmacologico mediante ablazione transcatetere con radiofrequenza.
La storia di questa sconvolgente modalità di trattamento
ablativo non chirurgico è iniziata in Europa 9 e da allora
si è dimostrata sempre più utile e terapia di
prima scelta per il controllo di quasi tutte le aritmie divenendo
spesso un trattamento curativo soprattutto nel campo delle aritmie
non necessariamente maligne.
Effetto proaritmico dei farmaci antiaritmici
Il potenziale effetto aritmogeno di un farmaco somministrato
agli effetti di controllare una aritmia era già noto
ai tempi di William Withering. Infatti un caso di effetto deleterio
legato a sovraccarico digitalico che si manifestava oltre che
con altri segni classici di intossicazione del farmaco anche
con aritmie era stato descritto nel lontanissimo 1779. Già
all’inizio del secolo scorso erano inoltre note le aritmie
ventricolari polimorfe che si presentavano nei soggetti in trattamento
chinidinico. Infatti alcuni casi di morti improvvisa e di sincope
legati al trattamento con chinidina potevano riconoscere un
simile meccanismo. E’ stato Dessertenne nel 1966 10 che
ha coniato il termine “torsades de pointes” (TP)
che oggi si utilizza diffusamente per l’aritmia ventricolare
polimorfa, spesso a risoluzione spontanea, tipica delle bradicardie
spiccate e del QT lungo. Quest’ultimo, più frequentemente
acquisito, compare a seguito di alterazioni disioniche o di
svariati trattamenti farmacologici fra cui spesso la chinidina.
Tale effetto proaritmico è favorito dalla bradicardia
perciò quando la chinidina è utilizzata per il
ripristino del ritmo sinusale nel caso della fibrillazione atriale
o per la sua profilassi, quando esso è solo parziale,
tale effetto si manifesta quasi esclusivamente al ripristino
del ritmo sinusale. Fra i farmaci antiaritmici quelli maggiormente
coinvolti in molte manifestazioni di proartimia sono quelli
della classe I, sia del gruppo A che C. Queste molecole (classe
IC) erano quelle coinvolte nella studio CAST che com’è
noto riguardava i pazienti con aritmie ventricolari post-infartuali.
L’incidenza sia di allungamento del QT che di aritmie
ventricolari del tipo TP è molto bassa per i farmaci
della classe III. Si consiglia comunque non solo di monitorare
molto attentamente l’intervallo del QT ma anche i livelli
di potassio e il perfetto compenso nei soggetti con insufficienza
cardiaca, di entrambi i sessi, in particolare se donne. Fra
i farmaci di questa classe, l’amiodarone potrebbe rappresentare
un valido prototipo di antiaritmico ideale se fosse possibile
minimizzare i suoi effetti collaterali. Alcuni fra i più
importati sono determinati dalla presenza di un quantitativo
ragguardevole di iodio nella molecola del farmaco. Ultimamente
si è cercato in tanti modi di ottenere altri validi antiaritmici
molto simili senza lo iodio ma al momento questi tentativi non
sono stati coronati da successo. Un temuto effetto collaterale
dell’amiodarone, per fortuna molto raro, ma non infrequente,
in particolare qualche tempo addietro, è rappresentata
dalla possibilità di avere fibrillazione ventricolare
in caso di somministrazione endovenosa del farmaco in soggetti
portatori di sindrome di Wolff-Parkinson-White e fibrillazione
atriale 11. In simili condizioni sia il verapamil che la digitale
sono controindicati in quanto l’allungamento della refrattarietà
del nodo atrioventricolare favorisce la penetrazione degli impulsi
anomali attraverso la via accessoria incrementando il “bombardamento”
subito a livello ventricolare dagli impulsi elettrici provenienti
dall’atrio.Vi sono alcuni riscontri a seguito di trattamento
di aritmie sopraventricolari con farmaci della classe IC che
a tutti gli effetti possono essere considerati effetti proaritmici.
Si possono verificare flutter atriali sincopali nei soggetti
nei quali la profilassi della loro fibrillazione atriale parossistica
viene eseguita anche con successo nei confronti della aritmia
per cui il trattamento è stato intrapreso; le sincopi
avvengono in questi casi per flutter atriale a conduzione atrioventricolare
1:1 attraverso il nodo atrioventricolare 12. Questo succede
in quanto i farmaci della classe I spesso hanno scarso o nullo
effetto elettrofisiologico diretto sulla suddetta struttura
nodale e il flutter “rallentato” farmacologicamente
viene condotto ai ventricoli a elevata frequenza. Il blocco
di branca funzionale che quasi sempre si associa all’elevata
frequenza, spesso è causa di erronea interpretazione
e il quadro viene descritto come da effetto proaritmico ventricolare.
Conclusioni
In questa sede non è stato possibile per ovvie ragioni
considerare tutti gli effetti proaritmici dei farmaci antiaritmici
e perciò mi sono limitato a trattare alcune delle manifestazioni
più frequenti di proaritmia. I farmaci antiaritmici sono
sempre estremamente utili ma vanno utilizzati con estrema saggezza
in quanto potenzialmente molto pericolosi. La terapia antiaritmica
farmacologica è sempre più una terapia di supporto
nel contesto di un trattamento ibrido che comprende anche diverse
modalità di trattamento non solo farmacologico ma anche
non-farmacologico e alcune volte la terapia antiaritmica farmacologia
va intesa come approccio terapeutico “ponte” verso
altre modalità di trattamento antiaritmico sia in forma
isolata che in associazione.
Per finire volevo ricordare a proposito dell’uso e abuso
dei farmaci antiaritmici quanto a questo proposito diceva di
Kaminetzky 13 : “There are not really ‘safe’
biologically active drugs. There are only ‘safe’
physicians. Questa è una affermazione che risale al 1963
e le cose nel frattempo stanno per fortuna cambiando.
BIBLIOGRAFIA
1.
Vaughan Williams EM: A classification of antiarrhythmic actions
reassessed after a decade of new drugs. J Clin Pharmacol 1984;
24: 129-35.
2. Harrison DC: Is there a rational basis for the modified classification
of antiarrhythmic drugs? In Morganroth J, Moore EN (eds). Cardiac
Arrhythmias . New therapeutic drugs and devices. Boston, Nijhoff
1985: 36-47.
3. Task Force of the Working Group on Arrhythmias of the European
Society of Cardiology. The Sicilian Gambit: A new approach to
the classification of antiarrhythmic drugs based on their actions
on arrhythmogenic mechanism. Circulation 1991; 84: 1831-45.
4. The Cardiac Arrhythmia Suppression Trial (CAST) Investigators:
Preliminary report: effect of encainide and flecainide on mortality
in a randomised trial of arrhythmia suppression after myocardial
infarction. N Engl J Med 1989; 321: 406-12.
5. Task Force of the Working Group on Arrhythmias of the European
Society of Cardiology: CAST and beyond. Implications of the
Cardiac Arrhythmia Suppression Trial. Circulation 1990; 81:
1123-7.
6. Prystowsky EN, Katz A, Knilans TK: Ventricular arrhythmias:
risk stratification and approach to therapy after the Cardiac
Arrhythmia Suppression Trial (CAST). PACE 1990; 13: 1480-7.
7. Greene HL, Roden DM, Katz RJ et al: The Cardiac Arrhythmia
Suppression Trial: first CAST…then CAST-II: JACC 1992;
19: 894-8.
8. Mirowski M, Reid PR, Mower MM et al: Termination of malignant
ventricular arrhythmias with an implanted automatic defibrillator
in human beings. N Engl J Med 1980; 303: 322-4.
9. Borggrefe M, Budde T, Podezeck A et al: High frequency alternating
current ablation of an accessory pathway in humans. JACC 1987;
10: 576-82.
10. Dessertenne F : Le tachycardie ventriculaire a deux foyes
oposes variables. Arch Mal Cœur 1966; 59: 263-9 .
11. Sheinman BD, Evans T: Acceleration of ventricular rate by
amiodarone in atrial fibrillation associated with Wolff-Parkinson-White
syndrome . BMJ 1982; 285: 999-1000.
12. Natham AW, Hellestrand KJ, Bexton RS, et al: Proarrhythmic
effects of new antiarrhythmic agent flecainide acetate. Am Heart
J 1984; 107: 222-9.
13. Kaminetzky HA: A drug on the market. Obstet Gynecol 1963;
21: 512-3.



